سرفصل های این مقاله
باتری های آلومینیوم هوا، اعم از اولیه و ثانویه، کاندیدای امیدوار کننده ای برای استفاده به عنوان باتری جهت تغذیه وسایل برقی و الکترونیکی، وسایل نقلیه کاربردی و تجاری و سایر موارد استفاده با هزینه نسبتا ًکمتر هستند. این مقاله تجزیه و تحلیل عملکرد این باتری ها را در مقایسه با سایر فناوری ها ارائه می دهد. همچنین هدف آن شناسایی موانع عمده ای است که باید برطرف شود.
آلیاژهای آلومینیوم دارای هزینه پایینی هستند و عملکردهای الکتروشیمیایی بهتری در مقایسه با آلومینیوم خالص ارائه می دهند. واکنش کاهش اکسیژن(ORR) در کاتد به طور معمول توسط کاتالیست های پلاتین و سایر عناصر نجیب کنترل می شود، اما مواد دیگری همچون: مواد کربنی، اکسیدهای فلزی انتقالی و کاتالیست های پایه پلیمری نیز عملکردهای امیدوار کننده ای از خود نشان داده اند.
اگرچه الکترولیت های پایه آبی قلیایی در حال حاضر به طور گسترده مورد استفاده قرار می گیرند، اما مواد الکترولیتی دیگری همچون الکترولیت های غیر آبی، مایعات آپروتیک و یونی برای باتری های اولیه و ثانویه جایگزین نیز قابل استفاده هستند.
مقدمه
در مسیر دستیابی به منابع انرژی پاک، همواره تلاش ها به سمت فناوری های قابل اطمینان تر و کارآمدتر بوده است. باتری های لیتیم یونی در حال حاضر بیشترین سهم را در بازار خودروهای برقی (EV) به خود اختصاص داده اند [۱]. با این حال، با توجه به نگرانی های ایمنی [۲]، محدوده کم پیمایش، ناپایداری لیتیوم در آب و هوای مرطوب [۳] و بازده الکتروشیمیایی پایین، نیاز به تحقیق در مورد سایر فناوری های باتری وجود امری مسلم است. در میان کاندیدهای احتمالی، باتری های فلز-هوا با چگالی انرژی بالا و استفاده از هوای محیط که باعث کاهش وزن آن ها شده یکی از بهترین و مناسب ترین گزینه های جایگزین است.
فلزاتی همچون لیتیم، روی، منیزیم، آلومینیوم، آهن و کلسیم عموما بیشترین استفاده را به عنوان آند در این باتری ها دارند. قبل از تجزیه و تحلیل عمیق باتری های آلومینیوم هوا، این باتری های فلز-هوا به طور خلاصه توضیح داده شده اند. چگالی انرژی ویژه نظری و ولتاژهای مدار باز (OCV) انواع مختلف سیستم های باتری درجدول ۱ آمده است.
جدول ۱- ولتاژ مدار باز باتری های فلز هوا
چگالی انرژی باتری های لیتیوم هوا در حدود ۵ تا ۱۰ برابر باتری های لیتیوم یونی است و بالاترین چگالی نظری انرژی، ۱۲ کیلووات ساعت بر کیلوگرم را از خود نشان می دهند [۴]. باتری های روی هوا دارای چگالی انرژی نظری ۱٫۳۵ کیلووات ساعت بر کیلوگرم و قابل شارژ هستند اما با چرخه عمر محدود [۵].
با این حال، مشکلات مربوط به این باتری عبارتند از (۱) تشکیل دندریت (که باعث اتصال کوتاه در باتری و ریختن فلز روی می شود) و(۲) اورولتاژ بالای بار برای واکنش کاهش اکسیژن (ORR) و واکنش تکامل اکسیژن (OER) که منجر به کاهش سرعت می شود. چگالی انرژی باتری های منیزیم هوا حدود ۶٫۵ کیلووات ساعت بر کیلوگرم و ولتاژ نظری آن ها حدود ۳٫۱ ولت است [۶].
چالش های اصلی این باتری نیز خوردگی آند و سرعت پایین واکنش ORR ست که منجر به بازده کولومبیک پایین در این باتری می شود. بیشتر باتری های منیزیم-هوا از نوع باتری های اولیه هستند و برای شارژ مجدد آن ها چالش های بزرگی وجود دارد. گزارشات اندکی [۷،۸] باتری های منیزیم هوای ثانویه را با الکترولیت های غیر آبی توصیف کرده اند.
باتری آلومینیوم هوا یک فناوری امیدبخش است که می تواند نیازهای انرژی پیش بینی شده آینبده را برآورده کند. چگالی انرژی عملی باتری آلومینیوم هوا تقریبا ۴٫۳۰کیلووات ساعت بر کیلوگرم است که از چگالی انرژی عملی باترهای لیتیوم هوا (۵٫۲۰ کیلووات ساعت بر کیلوگرم) کمتر و از چگالی انرژی عملی باتری های روی هوا (۱٫۰۸ کیلووات ساعت بر کیلوگرم) بیشتر است [۴،۹].
یک مطالعه ترمودینامیکی توسط لونتز و همکاران [۱۰] نشان داده است که حداکثر پتانسیل مدار باز آند آلومینیوم می تواند -۱٫۸۷ ولت در مقابل الکترود استاندارد هیدروژن در pH 14.6 به جای -۲٫۳۴ولت که به طور گسترده ذکر شده، باشد.
باتری های مبتنی بر آلومینیوم ممکن است صرفه جویی قابل توجهی در هزینه ها و بهبود ایمنی نسبت به باتری های لیتیوم یونی داشته باشند زیرا دارای واکنش پذیری کمتر، جابجایی آسان و ایمنی بیشتر هستند.
باتری های آلومینیومی هوا با استفاده از الکترولیت های آبی، آلی، مایع یونی (IL) و الکترولیت های بر پایه ژل پلیمری طراحی شده اند. باتری های آلومینیوم هوا با الکترولیت های IL دارای ویژگی های قابل شارژ هستند. الکترولیت های ژل پلیمری مشکلات مربوط به نشتی سیستم های باتری را با استفاده از الکترولیت های مایع برطرف می کنند اما چگالی انرژی کمتری تولید می کنند.
باتوجه به مطالب فوق واضح است که باتری آلومینیوم هوا به طور منحصر به فردی در بین سیستم های باتری فلز-هوا قرار گرفته است. مزایای کلیدی باتری آلومینیومی هوا عبارتند از (۱): چگالی انرژی آن ها پنج تا ده برابر باتری های لیتیم یونی است، (۲) آند آلومینیوم بسیار سبک است (کاتد به طور موثر به یک شبکه سیم و لایه غشایی کاهش می یابد)، ارزان، غیر سمی و ایمن است، (۳) زوج های کاهنده مبتنی برآلومینیوم ظرفیت ذخیره سازی بسیار بالاتری را ارائه می دهند (۴) ظرفیت معادل الکتروشیمیایی آلومینیوم (۲٫۹۸ Ah/gr) بسیار کمتر از لیتیم (۳٫۸۶ Ah/gr) و سایر فلزات است، (۵) آلومینیوم را می توان به راحتی بازیافت کرد.
با این حال، توسعه باتری های قابل دوام آلومینیوم هوا، که برای مصرف کنندگان نیز قابل قبول باشد، نیاز به رفع مشکلاتی دارد که امروزه توسط تکنسین های باتری آلومینیوم هوا مطرح شده است. این مشکلات عبارتند از (۱) سرعت بالای خود خوردگی آلومینیوم در محلول های قلیایی در هر دو حالت مدار باز و در حالت تخلیه، (۲) محصولات جانبی مانند Al2O3 و Al (OH) 3 در آند و کاتد (۳) ماهیت پیچیده تداخل سه ظرفیتی Al3+ در کاتد، (۴) ماهیت برگشت ناپذیر تشکیل آلومینای هیدراته، (۵) از دست دادن سریع شارژ در انبار که منجر به ماندگاری ناچیز می شود. داگلاس پی هارت و بسیاری از کارشناسان معتقدند که باتری های آلومینیوم هوا در آینده باید دارای انرژی ویژه ی زیادی باشند.
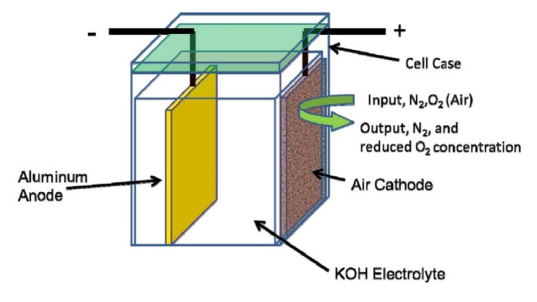
بررسی های زیادی در مورد باتری های آلومینیوم هوا [۹،۱۱-۱۶] انجام شده است که بر روی اجزای باتری شامل آند، کاتد و الکترولیت تمرکز کرده اند. مرور حاضر سعی بر طراحی و مونتاژ (شکل ۱) باتری آلومینیوم هوا و مقایسه آن با سایر فناوری های باتری، جدا از به روزرسانی اجزای باتری تمرکز کند. هدف این بررسی جعبه ابزاری برای مونتاژ باتری آلومینیومی هوا است. قابلیت سوددهی اقتصادی و ورود به بازار اصلی ترین دغدغه ای است که در آن باید جدای از تحقیقات علمی، وضعیت فناوری موجود، هزینه مواد خام و سهولت ساخت را در نظر گرفت.
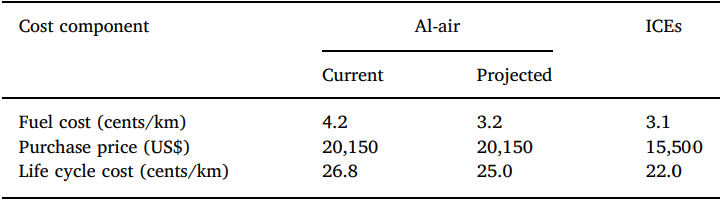
اجازه دهید نگاهی به اقتصاد باتری EV داشته باشیم. هزینه تمام شده باتری در حال حاضر ۴٫۲ سنت/کیلومتر و پیش بینی شده ۳٫۲ سنت/کیلومتر شود [۱۷]. این عدد با هزینه موتورهای احتراق داخلی (ICEs) که هزینه سوخت فعلی آن ها ۳٫۱ سنت/کیلومتر بر اساس جدول ۲ است، قابل مقایسه است.
جدول ۲- مقایسه هزینه باتری های آلومینیوم هوا و موتورهای احتراق داخلی (ICEs)
قیمت خرید ماشین های الکتریکی آلومینیوم هوا در حال حاضر حدود ۲۵ درصد بیشتر از ICE ها است، این امر هزینه چرخه عمر ICE ها و ماشین های الکتریکی آلومینیوم هوا را ۲۲٫۰ سنت/کیلومتر و ۲۶٫۸ سنت/کیلومتر (فعلی) و ۲۵٫۰ سنت/کیلومتر اعلام می کند (پیش بینی شده). علاوه بر این، ICE ها از نظر تحقیقاتی به بلوغ رسیده اند در حالی که باتری های آلومینیوم هوا هنوز به مرحله تکامل نرسیده اند.
با در نظر گرفتن جرم مشابه ۱۰۸۸ کیلوگرم برای هر دو نوع Al -air و ICE در وسیله نقلیه ای که قادر به پیمایش ۴۰۰ کیلومتر هستند، ماشین الکتریکی آلومینیوم هوا، با تحقیقات بیشتر، می تواند جایگزین بالقوه ای برای ICE باشد.
واکنش های الکتروشیمیایی باتری های آلومینیوم هوا به شرح زیر است:
در آند: Al(s)+3OH^- (aq)→Al〖(OH)〗_۳ (s)+3e^- -2.35V
در کاتد: O_2 (g)+2H_2 O(l)+4e^-→۴OH^- (aq) +0/40 V
به طور کلی: ۴Al(s)+3O_2 (g)+6H_2 O(l)→۴Al〖(OH)〗_۳ (s) -2.75V
۲٫ آند
آلومینیوم به دلیل چگالی بالای انرژی، پتانسیل بار منفی، قابلیت بازیافت و فراوانی، سال هاست که به عنوان آند در باتری های فلز-هوا و فلز-یون مورد استفاده قرار می گیرند. این نوع باتری بیش از ۶۰ سال است که تولید می شود و همچنین به راحتی در دسترس است.
آلومینیوم های تجاری موجود، ۲N5 (99.5٪ خلوص) ۴N (99.99٪ خلوص) هر دو به عنوان آند استفاده شده است. ناخالصی های موجود در آند آلومینیوم و محصولات ایجاد شده در طول واکنش های آندی لایه هایی را تشکیل می دهند که مانع عملکرد باتری می شوند [۱۸].
با این حال، درجه Al 2N5 یک آند مناسب برای شرایط تخلیه قدرت بالا است. مشاهده شده است [۱۷] که درجه ۲N5 و ۴N در بازار موجود آلومینیوم در درجات مختلف با مشکلات ناشی از (۱) خوردگی باعث تولید محصولات Al (OH)4- و Al(OH)3 می شود، (۲) تکامل هیدروژن ناشی از این واکنش های جانبی که توسط معادله ارائه شده است، Al+3H2O→Al(OH)3+3/2H2 و (۳) غیرفعال شدن با تشکیل یک فیلم اکسیدی تقریباً آنی هنگام ورود به هوا یا آب.
خود فرآیند ساخت نیز می تواند بر رسانایی آند آلومینیوم تأثیر بگذارد، به عنوان مثال، اتصال دهنده هایی مانند ترپینئول می توانند بر رسانایی آند آلومینیوم تأثیر منفی بگذارند. بنابراین، کلوخه سازی لیزری یک روش ترجیحی است که می تواند آندهای آلومینیوم را به روش غیر تهاجمی و دقیق بسازد. در یک مطالعه [۱۹] به بررسی تاثیر سینترینگ لیزری پرداخته شده است که در ان میزان جریان از ۲mAh/gr به ۱۲۱mAh/gr بهبود یافته است.
همچنین لازم است در فرایند بررسی آند آلومینیوم، اندازه دانه و جهت بلورهای آن نیز در نظر گرفته شود. ساختار دانه های ریزتر آند آلومینیوم عملکرد باتری بهتری نسبت به ساختار دانه درشت دارد. با کاهش اندازه دانه، خاصیت ضد خوردگی و فعالیت الکتروشیمیایی آند آلومینیوم افزایش می یابد.
فن و لو [۲۰] ریزساختار نمونه های مختلف آلومینیوم اکسترود شده را با استفاده از انالیز (EBSD) تجزیه و تحلیل کردند (شکل ۲) و پیشنهاد کردند که افزایش تعداد عبورها، اندازه دانه ها را کاهش می دهد، که مستقیما ًبا کاهش تکامل هیدروژن متناسب است. آلومینیوم ناهمسانگرد به دلیل نقص کریستالی بهتر از آلومینیوم پلی کریستالی عمل می کند (شکل ۳). صفحه کریستالی (۰۰۱) کمترین میزان خوردگی را نشان داده و بیشترین چگالی ظرفیت (۲۵۴۱ mAh/gr) را به دلیل کمترین انرژی سطحی می دهد [۲۱].
شکل ۲٫ تجزیه و تحلیل پراکندگی الکترونی (EBSD) نقشه مرز دانه ها، نقشه های جهت گیری و {۱۱۱} اشکال قطب ها پس از گذرهای مختلف فشار زاویه ای کانال برابر (ECAP): (الف) ریخته گری (ب) ۳ پاس (ج) ۵ پاس (د) ۷ پاس (ه) ۹ پاس [۲۰].
شکل ۳٫ رفتار تخلیه باتری آلومینیومی هوا بر اساس آندهای آلومینیوم تک کریستالی و چند کریستالی در چگالی جریان ۱۰ میلی آمپر بر سانتی متر در ۴ M KOH [21].
۲٫۱ آلیاژهای آلومینیوم
آلومینیوم خالص، هنگامی که به عنوان آند در حضور الکترولیت آبی استفاده می شود، به سرعت دچار خوردگی می شود و واکنش شدیدی برای تولید هیدروژن انجام می دهد [۲۲]. آلیاژهای آلومینیوم برای غلبه بر محدودیت های آلومینیوم خالص و همچنین بهبود کارایی الکتروشیمیایی آند مورد مطالعه قرار گرفته اند.
عناصر مختلف مانند گالیم، تیتانیم، ایندیم، و قلع به عنوان عناصر آلیاژی در ترکیب آلیاژهای آلومینیوم در نظر گرفته شده اند. روی معمولا برای کاهش خوردگی آند با افزایش پتانسیل تکامل هیدروژن استفاده می شود.
پارک و همکاران [۲۳] آلیاژهای روی-آلومینیوم را به عنوان آند آزمایش کرده و خاطرنشان کردند که این آلیاژ زمان تثبیت ولتاژ کوتاه تری نسبت به آلومینیوم خالص ۴N دارد. همچنین، میزان خوردگی بالاتری را نشان می دهد که به وجود آهن و سیلیسیم نسبت داده می شود (آلومینیوم استفاده شده برای آلیاژ ۹۹٫۷۵ درصد در مقایسه با ۹۹٫۹۹ درصد بود).
بنابراین، افزایش خوردگی توسط آهن و سیلیسیم اثرات سودمند روی را تحت الشعاع قرار داده است. علاوه بر این، آلیاژهای روی-آلومینیوم تشکیل دو لایه اکسیداسیون، نوع ۱ (شامل Zn(OH)2 متخلخل و ZnO معیوب) و نوع ۲ (شامل ZnO محافظ) را نشان دادند. لایه نوع ۲ عملکرد تخلیه باتری را کاهش می دهد. این اثر لایه غیرفعال را می توان با مصرف آلیاژ ایندیم-روی-آلومینیوم کاهش داد، که نه تنها ارزان تر است بلکه با مهار تشکیل فیلم نوع ۲، عملکرد باتری را نیز بهبود می بخشد.
عملکرد آندهای (wt%) Al -1Mg -0.1Ga -0.1Sn و Al -1Mg -1Zn -0.1Ga -0.1Sn (wt%) نیز مورد مطالعه قرار گرفت [۲۴]. اهمیت روی به عنوان یک عنصر آلیاژی مشخص شد زیرا آلیاژهای حاوی روی، عملکرد الکتروشیمیایی بهتر و همچنین میزان خوردگی کمتری را نشان می دهد.
عنصر سرب با افزایش اورولتاژ تکامل هیدروژن، تکامل هیدروژن را کاهش می دهد. علاوه بر این [۲۵]، گالیم فیلم اکسید را مهار می کند و در نتیجه آلومینیوم را فعال می کند، به ویژه در محلول NaCl، جایی که می تواند با جذب یون های Cl- ، سایت های آلومینیوم را فعال کند [۲۶].
آندهای Al -Bi -Pb -Ga (ترکیب وزن ۰٫۱۵Bi -0.15Pb -0.035Ga -Al (wt%)) [27] همچنین نتایج امیدوارکننده ای با چگالی توان حداکثر بیش از دو برابر آلومینیوم خالص، راندمان آندی بالاتر و مقاومت انتقال بار کوچکتر (برای محلول ۲ مولار NaCl) نشان داده شده است.
در محلول KOH، این آلیاژ به دلیل سرب، بیسموت و گالیم که باعث تکامل هیدروژن بیش از حد می شود، میزان خوردگی کمتری را در مقایسه با آلومینیوم خالص می دهد. به طور مشابه، یک آلیاژ چهارگانه آلومینیوم (خلوص ۹۹٫۸ درصد) حاوی سرب، گالیم و ایندیم نرخ های خوردگی قابل مقایسه و پتانسیل های مدار باز را در آلومینیوم فوق خالص ( ۹۹٫۹۹ درصد) در شرایط آزمایش مشابه، نشان می دهد که آلیاژسازی برای نشان دادن نتایج پایداراست [۲۸,۲۹].
آلیاژ امیدبخشی که برای این باتری مورد استفاده قرار می گیرد، آلیاژ آلومینیوم-T7351 7075 که توسط مس پوشش داده شده است، (۵٫۶-۶٫۱ Zn, 2.1-2.5 Mg, 1.2-1.6 Cu, <0.5 Si, Fe, Mn, Ti, Cr (wt%)) [30]. مس با رسوب الکتروشیمیایی منجر به ایجاد یک لایه همگن جذب شده می شود که با ایجاد مانع با محلول، سرعت تکامل هیدروژن را کاهش می دهد. این مزاحمت، کارایی آلومینیوم را به عنوان یک آند مختل نمی کند. مس، در واقع، فعالیت تخلیه را بهبود می بخشد و پتانسیل باتری را با کاهش مقاومت آندی افزایش می دهد (جدول ۳).
جدول ۳- پتانسیل های سلول آندی برای آلیاژهای مختلف آلومینیوم در NaOH 4M و mA/cm220
بدیهی است که آلیاژهای آلومینیوم نه تنها نسبت توان به هزینه بالاتری نسبت آلومینیوم خالص ارائه می دهند بلکه میزان تکامل هیدروژن و خوردگی را نیز کاهش می دهند. وجود روی همراه با عدم وجود آهن و سیلیسیم باعث افزایش کارایی باتری می شود. بهبود فناوری مربوط به فرایند ساخت، مانند کلوخه سازی، می تواند عملکرد آند را به شدت بهبود بخشد. تلاش های بیشتری برای کاهش هزینه ساخت و افزایش تولید این آلیاژها لازم است تا این آلیاژها بتوانند جایگزین Al 4N خالص به عنوان آند شوند.
۳٫ کاتد
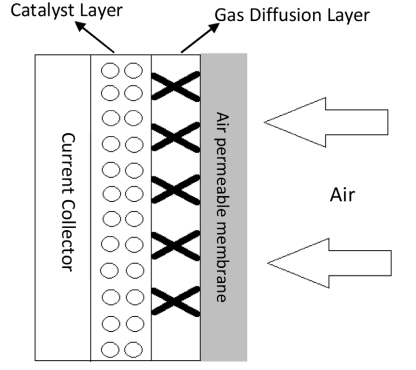
کاتد هوا شامل یک کاتالیست کاهش اکسیژن، یک جمع کننده جریان و یک الکترود کامپوزیت است (شکل۴). این الکترود از یک لایه انتشار گاز (GDL)و یک فیلم پلیمری آبگریز مانند پلی تترا فلورو اتیلن (PTFE)یا پلی وینیلیدن دی فلوراید (PVdF) تشکیل شده است.
این فیلم مواد را متصل کرده و همچنین از نفوذ الکترولیت به داخل الکترود جلوگیری می کند[۳۱]. جمع کننده جریان معمولا ًیک صفحه یا چشمه ساخته شده از نیکل است که قدرت مکانیکی را به سلول منتقل می کند و از انتقال الکترون ها پشتیبانی می کند [۳۲].
شکل ۴٫ ساختار کاتد هوا
باتری های آلومینیوم هوا عمدتا به دلیل سرعت پایین واکنش احیای اکسیژن (ORR) که در کاتد انجام می شود تجاری نشده و مورد استفاده قرار نگرفته اند. طراحی و مونتاژ مناسب کاتد به همراه ترکیب الکتروکاتالیست مناسب برای تغییر فعالیت ORR یکی از موثرترین کارهایی است که باید انجام شود تا باتری های آلومینیوم هوا قابل استفاده شوند.
از آنجا که شیمی واکنش های صورت گرفته در سلول های روی-هوا ، لیتیم-هوا و سلولهای سوختی غشای پلیمری الکترولیت (PEMFC)است، تحقیقات صورت گرفته در مورد واکنشهای کاهش اکسیژن در این سلول ها می تواند بر روی کاتد هوای باتری آلومینیومی هوا نیز اعمال شود.
۴٫ الکترولیت ها
الکترولیت یک محیط رسانا است که اجازه حرکت یون ها از کاتد به آند را می دهد. الکترولیت تکامل هیدروژن و واکنش های بارشی در آند آلومینیوم را کنترل می کند و همچنین پتانسیل کلی سلول را تعیین می کند.
تحقیقات در مورد باتری آلومینیوم هوا برای استفاده از الکترولیت های آبی، غیر آبی، مخلوط و آپروتیک متمرکز شده است. در این بخش، تمرکز ما بر الکترولیت های فعلی و همچنین کلاس های جدیدی است که برای باتری های آلومینیوم هوا بررسی شده است.
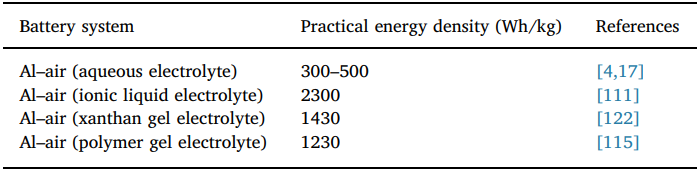
مواد افزودنی به الکترولیت ها برای بهبود استفاده از آند و کاهش تکامل هیدروژن نیز مورد بحث قرار می گیرد. خلاصه ای از چگالی انرژی باتری های آلومینیومی هوا با الکترولیت های مختلف درجدول ۴ گردآوری شده است.
جدول ۴ چگالی انرژی باتری های آلومینیوم هوا با استفاده از الکترولیت های مختلف.
۴٫۱٫ الکترولیت های آبی
الکترولیت های آبی قلیایی به طور گسترده ای به عنوان الکترولیت برای باتری های آلومینیومی هوا استفاده می شوند و بیش از نیم قرن مورد مطالعه قرار گرفته اند [۱۱۶و۱۱۵]. KOH و NaOH بیشترین کاربرد را در بین الکترولیت هاسی قلیایی دارند. این الکترولیت ها دارای ویژگی هایی همچون هدایت یونی بالا، اورولتاژ پایین، غیر سمی بودن و ORR سریع را دارا هستند [۱۴].
کاپالی و همکاران [۲۶] الکترولیت های قلیایی را بطور سیستماتیک برای باتری های آلومینیوم هوا تجزیه و تحلیل کرده اند. الکترولیت های قلیایی حاوی سیترات، استاننات و کلسیم دارای بیشترین میزان حلالیت آلومینیوم ، کمترین میزان خوردگی و بالاترین OCV را نشان داده اند.
همچنین غلظت های مختلف اجزای منفرد – استنات ها، اندات ها، گالات ها، منگنات ها، مورد آزمایش قرار گرفتند. نتایج نشان دادند که منگنات پتاسیم (غلظت ۳-۱۰ مولار) با بازدهی کولمبیک بالای ۹۰ درصد و نرخ خوردگی مشابه سایر عوامل؛ به عنوان موثرترین عامل شناخته [۱۱۸و۱۱۷].
در میان سیستمهای دوتایی ، گالات + ایندات، منگنات + ایندات، بیسموتات + استاننات و استاننات + ایندات، استنات + هیدروکسید ایندیوم (Na2SnO3 + In(OH)3) در بین ردیف بهترین ها بودند (بازده کولومبیک تا ۹۶ درصد و کاهش قابل توجه در میزان خوردگی ). با این حال، مشکلات عمده مربوط به الکترولیت های قلیایی آبی عبارتند از تبخیر آب، چگالی انرژی پایین و کربناسیون الکترولیت که مانع دسترسی هوا به کاتدها می شود [۱۳[.
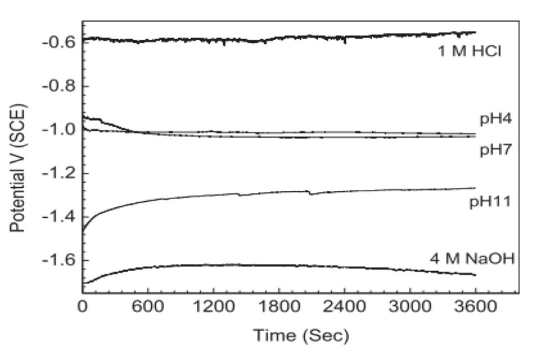
شکل ۵ تکامل پتانسیل مدار باز در مقابل زمان در محلول های مختلف برای نمونه های آلیاژ [۱۲۸[.
الکترولیت های خنثی نمک برای اولین بار در یک اختراع در ۱۹۷۵ (US3887399A) ثبت شد. مطالعات متعدد استفاده از الکترولیت نمکی با پتانسیل در محدوده ۰٫۶۵-۱٫۱ ولت را ثبت کرده اند [۱۲۴-۱۱۹].
در مقام مقایسه، الکترولیت های خنثی عملکرد کمتری را نسبت به الکترولیت های قلیایی از خود نشان داده اند (چگالی انرژی در الکترولیت خنثی یک سوم الکترولیت قلیایی بود [۱۲۵]. الکترولیت های خنثی (به ویژه نمک سدیم) عمدتا به دلیل کاربرد بالقوه آن ها در باتری های فلز-هوا در وسایل نقلیه دریایی که می توانند مستقیما ًاز آب دریا استفاده کنند، قابل توجه هستند و مطالعات نشان داده اند که می توانند به عنوان منابع قدرت متوسط و بزرگ برای کاربردهای دریایی مورد استفاده قرار گیرند [۱۲۶].
الکترولیت های اسیدی مزایا و معایب خود را دارند که مهمترین آن ها حذف کربناسیون است. وقتی H2So4 3 مولار با HCl 0.04 مولار به عنوان الکترولیت مورد استفاده قرار گرفت، سپس OCV در مقایسه با الکترولیت های KOH و NaOH مثبت تر بود [۱۲۷].
این نتایج با مطالعات Ma و همکاران بیشتر تأیید می شود [۱۲۹،۱۲۸] جایی که OCV با کاهش pH الکترولیت کاهش می یابد (شکل ۵). این مقاله همچنین درک مکانیسم خوردگی در محلول های قلیایی و اسیدی را ارائه می دهد. محلول های اسیدی باعث خوردگی آلومینیوماز نوع پیتینگ می شوند، در حاالی که محلول های قلیایی باعث خوردگی کریستالوگرافی می شوند[۱۳۰]. از طرفی الکترولیت های اسیدی سرعت خوردگی کمتری نسبت به الکترولیت های قلیایی دارند.
۴٫۱٫۱٫ افزودنی های الکترولیت های آبی
افزودن مواد افزودنی به الکترولیت های آبی به طور کلی (۱) خوردگی جانبی آلومینیوم را سرکوب می کند، (۲) تکامل هیدروژن را کاهش می دهد و (۳) میزان استفاده از آند را افزایش می دهد. در حالی که هر سه عملکرد به هم مرتبط هستند، به نظر ، اساسی ترین عملکرد آنها کاهش خوردگی آند آلومینیوم باشد.
افزودنی های آلی و معدنی مختلفی را می توان به الکترولیت های آبی اضافه کرد. از جمله این افزودنی ها می توان به ۸هیدروکسی کینولین و کمپلکس ZnO [131]، -۱آلیل-۳-متیل آمیدازولیوم بیس (تری فلورومتیل سولفونیل) ایمید (IL) [132]، کربوکسی متیل سلولز و ZnO[133] ، اسیدهای دی کربوکسیلیک [۱۳۴] و ال-سیستئین و نیترات سریم [۱۳۵] اشاره کرد. ًبر اساس میزان تکامل هیدروژن، افزودنی مایع یونی کمترین میزان تکامل گاز هیدروژن را با سرعت کمتر از ۰٫۱ میلی لیتر در دقیقه بر سانتی متر مربع برای غلظت بیشتر از ۱ میلی مولار ارائه می دهد.
۴٫۲٫ الکترولیت های غیر آبی
الکترولیت های غیر آبی محدودیت های سیستم های آبی را بر طرف میکنند. از جمله مزایای آن می توان به چگالی انرژی بالاتر، جلوگیری از خوردگی آندی و ولتاژ بیشتر باتری اشاره کرد[۱۲] همچنین در این نوع الکترولیت ها، مشکل از دست دادن رسانایی یونی ناشی از واکنش های بارش را می توان به راحتی حل کرد. الکترولیت های غیر آبی را می توان به (۱( الکترولیت های آپروتیک و (۲) الکترولیت های پلیمری طبقه بندی کرد.
الکترولیتهای آپروتیک معمولا ًبرای باتری های لیتیوم هوا استفاده می شوند [۱۳۹و۱۳۷] و این پتانسیل را دارند که در سیستم های باتری آلومینیوم هوا مورد استفاده قرا گیرند. برای اولین بار در سال ۲۰۱۳ [۱۴۰]، مشخص شد که ، مایعات یونی دمای اتاق (RTIL) مانند EMIm(HF0)2.3F به عنوان یک مهار کننده عالی برای خوردگی می توانند به کار روند و چگالی انرژی بالایی (۲٫۳ کیلووات ساعت بر کیلوگرم) را نیز فراهم می کنند. مایعات یونی دارای رسانایی بالا، ثبات شیمیایی و ویسکوزیته پایینی هستند.
الکترولیت های پلیمری در اصل جداکننده های آندی و کاتدی هستند که یک الکترولیت ( مانند KOH) را جذب کرده و اختلاف پتانسیل را در باتری حفظ می کنند. به طور معمول، آن ها فیلم های نازکی هستند که با استفاده از روش های ریخته گری پلیمر، تبخیر حلال و روش های رسوب اسپری تهیه می شوند. الکترولیت پلیمر جامد (SPEs )PAA/PVA که با آلومینیوم هوا استفاده می شود، چگالی توان ۱٫۲ میلی وات بر سانتی متر مربع دارد که نسبت به روی هوا کمتر است که احتمالا ًبه دلیل غیرفعال شدن سطح آلومینیوم است [۱۴۵].
الکترولیت های ژل پلیمری (PGEs) که برای باتری های فلز-هوا توسعه یافته اند، محلول های آبی مانند KOH را جذب می کنند تا ژلی بر پایه پلیمر تولید کنند که رسانایی یونی خوبی دارد. از جمله مزایای PGEs می توان به توانایی کنترل نشت الکترولیت، پایداری حرارتی و الکتروشیمیایی اشاره کرد.
۵٫ طراحی و مونتاژ باتری های آلومینیومی هوا
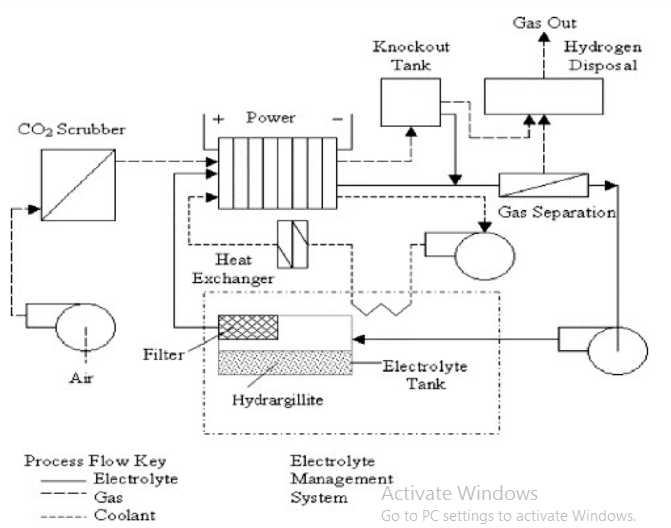
طراحی و مونتاژ مناسب باتری آلومینیوم هوا می تواند باعث افزایش کارایی، افزایش عمر باتری و ماندگاری بیشتر شود. یک سیستم باتری در حال کار دارای اجزای زیر است: باتری آلومینیوم هوا ، یک کریستال ساز برای کنترل ترکیب الکترولیت ، جاذب ۲CO، جدا کننده گاز برای جدا کردن هیدروژن از الکترولیت و یک سیستم خنک کننده برای کنترل حرارت. نمای شماتیک این مجموعه در شکل ۶ آورده شده است [۱۵۴].
مشکل اصلی در طراحی باتری آلومینیوم هوا عمر کوتاه سلول و از دست دادن سریع شارژ آن است. برای افزایش طول عمر سلول، می توان الکترولیت را با یک روغن اولئوفوبیک جابجا کرد که خوردگی آند را در حالت آماده به کار متوقف می کند [۱۵۵].
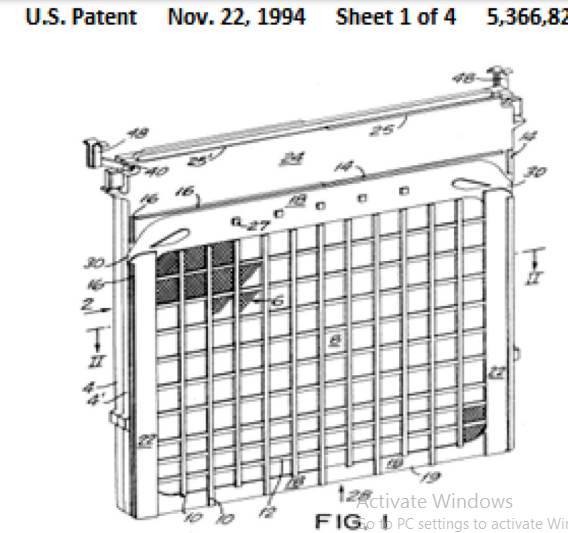
باتری آلومینیوم هوا با طراحی مکانیزم کشویی [۱۵۰] هنگامی که از آن استفاده نمی شود، آند آلومینیوم را از الکترولیت حذف می کند. ثبت اختراعات تجاری روی باتری های فلز- هوا، ساختارهای متفاوتی را ارائه کرده است. ثبت اختراع ۱۹۹۴ (شکل ۷) یک سلول ماژولار برای سیستم باتری چند سلولی را توصیف می کند که در هر دو انتهای آن کاتدهای هوا و سایر اجزای آن در وسط قرار گرفته است. در سال ۱۹۹۹، یک بسته بندی باتری برای استفاده در تلفن های همراه ثبت شد .(US6517967B1)
شکل ۶٫ نمودار جریان اصلی سیستم باتری آلومینیومی هوا [۱۵۴].
شکل ۷٫ US4925744A
۶٫ نتیجه گیری
باتری های آلومینیوم هوا می توانند نیازهای مصرف کننده را برآورده کنند. طیف گسترده ای از کاربردها (از وسایل نقلیه گرفته تا سیستم های دریایی)، واکنش های بی خطر محیطی، استفاده از هوای محیط و فراوانی آلومینیوم، باتری آلومینیوم هوا را به منبع انرژی امیدوار کننده ای برای نسل آینده تبدیل کرده است. با این حال، در حال حاضر فناوری باتری آلومینیوم هوا هنوز نیاز مطالعه و به خصوص مطالعات افزایش مقیاس برای الکترود و کاتد دارد.
در این سیستم مشکلات خاصی وجود دارد که مربوط به ذات باتری است، از جمله این مسائل می توان به خوردگی آند، انسداد منافذ، ORR ضعیف برای کاتد، کربناسیون در الکترولیت های آبی، عدم وجود روش مشخص برای جایگزینی آند در باتری های اولیه اشاره کرد.
در حال حاضر، آلیاژهای آلومینیومی زیادی وجود دارند که هر کدام مزایای خاص خود را دارند. مواد کربنی برای استفاده به عنوان کاتالیست در کاتدها جزو جذاب ترین و بهترین موارد هستند، به ویژه با توجه به تنوع و هزینه نسبتا پایین آن ها. الکترولیت های مورد استفاده در این باتری ها به طور معمول KOH هستند. الکترولیت های پلیمری حالت جامد و مایعات یونی نیز پتانسیل بالایی برای استفاده به عنوان الکترولیت از خود نشان داده اند.



![باتری های آلومینیوم هوا: مروری بر قابلیت زنده ماندن 4 شکل 2. تجزیه و تحلیل پراکندگی الکترونی (EBSD) نقشه مرز دانه ها، نقشه های جهت گیری و {111} اشکال قطبها پس از گذرهای مختلف فشار زاویه ای کانال برابر (ECAP): (الف) ریخته گری (ب) 3 پاس (ج) 5 پاس (د) 7 پاس (ه) 9 پاس [20].](https://saniva.co/wp-content/uploads/2021/11/8.png)
![باتری های آلومینیوم هوا: مروری بر قابلیت زنده ماندن 5 رفتار تخلیه باتری آلومینیومی هوا بر اساس آندهای آلومینیوم تک کریستالی و چند کریستالی در چگالی جریان 10 میلی آمپر بر سانتی متر در 4 M KOH [21].](https://saniva.co/wp-content/uploads/2021/11/7.png)









1 دیدگاه
[…] باتری آلومینیوم هوا […]